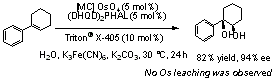1 0 0 0 OA アダマンタンの不斉修飾法の開発と活用
- 著者
- 澁谷 正俊 富澤 正樹 高橋 道康 谷口 孝彦 小笠原 國郎 岩渕 好治
- 出版者
- 日本薬学会化学系薬学部会
- 雑誌
- 反応と合成の進歩シンポジウム 発表要旨概要 第29回反応と合成の進歩シンポジウム
- 巻号頁・発行日
- pp.212-213, 2003-09-24 (Released:2004-03-16)
ダイヤモンドの基本構成単位に相当する高度な対称性を有する三環性脂環式炭化水素:アダマンタンは医薬品素材として極めて重要な位置を占めている。例えば、パーキンソン病治療薬ならびにA 型インフルエンザ予防薬であるアマンタジンを始め、合成レチノイド、NMDA 型グルタミン酸受容体アンタゴニスト、抗腫瘍剤など多様な薬剤分子の生理活性発現に関与している。アダマンタンは創薬化学における有用素子として、その官能基化と誘導体化に関する研究が盛んに行われているが、意外にもその分子上へのキラルな要素の導入に関しては、広瀬らの豚肝臓アルコールデヒドロゲナーゼを用いた置換2-アダマンタノンの不斉還元ただ一例が知られるのみであった。我々は、アダマンタンの創薬資源としてのさらなる可能性に興味を抱き、その母核上へのエナンチオ制御下の効率的官能基導入法を開発すべく検討を開始した。その結果、入手容易なσ-対称性7-メチレンビシクロ[3.3.1]ノナン-3-オンのエナンチオ特異的修飾と、その生成物のアダマンタン核への閉環という2つの工程を鍵として、アダマンタンの不斉修飾への途を拓くことができた(Scheme 1)。本シンポジウムでは、その経緯とともに本手法のキラルα-アダマンチル-α-アミノ酸合成への活用について報告したい。【7-メチレンビシクロ[3.3.1]ノナン-3-オンのエナンチオ選択的修飾】村岡らの報告に従って合成した7-メチレンビシクロ[3.3.1]ノナン-3-オンのケトン部周辺へのエナンチオ選択的な官能基の導入を検討した。キラルリチウムエノラートを生成後、ベンズアルデヒドとの不斉アルドール反応を行ったところ、シリカゲルカラムクロマトグラフィーにより分離可能な2 種のジアステレオマー混合物(生成比10:1)が得られた。収率79%、89% ee で得られる主成績体は一回の再結晶によって、光学的に純粋とすることができた。一方、エキソメチレン部を足場とするエナンチオ非対称化については未だ良好な結果を得るには至ってないが、エキソメチレン体から4 工程を経て導かれるラセミアリルアルコールが香月–Sharpless 不斉エポキシ化反応下に速度論的分割を受け、高光学純度(96%ee)のアリルアルコールを与えることを見いだした(Scheme 2 )。【7-メチレンビシクロ[3.3.1]ノナン-3-オン誘導体のアダマンタンへの閉環反応】上述のようにして得た7-メチレンビシクロ[3.3.1]ノナン-3-オン誘導体を基質として、Olah らの条件に準じてアダマンタンへの閉環反応を検討した。その結果、いずれの場合も0.35 当量の四塩化チタン存在下、塩化メチレン中、–30℃で速やかに閉環反応は進行し、光学活性なアダマンタン誘導体を与えた(Scheme 3 )。ここで、アダマンタン核への多様な官能基導入法の開発という観点から、オキシムエーテルへと導き、このものの閉環反応を検討した。その結果、オキシムエーテルもケトン体と同様にルイス酸条件下、種々のヘテロ原子求核剤と速やかに反応して良好な収率で1,3-置換アダマンタン誘導体を与えることを見いだした。【キラルα-アダマンチル-α-アミノ酸の合成】アルドール成績体を光延条件下アジドへと変換した後、閉環条件に付し、高収率でアダマンタンを得た。アミノ基への還元、保護、ベンゼン環の酸化を経てキラルα-アダマンチル-α-アミノ酸を合成した(Scheme 5)。また、キラルシリルエノールエーテルとイミンとのMannich 反応と閉環反応の組み合わせによる短工程合成も達成した(Scheme 6)。
1 0 0 0 OA リゼルグ酸および関連アルカロイドの不斉全合成
- 著者
- 岩田 顕 井貫 晋輔 大石 真也 藤井 信孝 大野 浩章
- 出版者
- 日本薬学会化学系薬学部会
- 雑誌
- 反応と合成の進歩シンポジウム 発表要旨概要 第37回反応と合成の進歩シンポジウム
- 巻号頁・発行日
- pp.164, 2011 (Released:2012-02-10)
The family of ergot alkaloids produced by the fungus Claviceps purpurea is one of the most intriguing classes of natural products because of their broad biological and pharmacological activities. Despite intensive synthetic investigations, most synthetic studies of the ergot alkaloids, particularly (+)-lysergic acid, (+)-lysergol and (+)-isolysergol, have relied on a stepwise linear approach for the construction of the C/D ring system. Recently, we developed a palladium-catalyzed domino cyclization of the racemic allenic amide to provide the tetracyclic core of ergot alkaloids. In this study, we constructed the chiral allenic amide via the two synthetic routes using aldehyde alkynylation/asymmetric hydrogenation or asymmetric epoxidation/regioselective reductive ring-opening reaction. Using the resulting chiral allenic amide , enantioselective total syntheses of (+)-lysergic acid, (+)-lysergol and (+)-isolysergol were accomplished.
1 0 0 0 クラブバイサイクロンの合成研究
- 著者
- 武口 俊太 川岸 貴博 伊藤 久央 井口 和男
- 出版者
- 日本薬学会化学系薬学部会
- 雑誌
- 反応と合成の進歩シンポジウム 発表要旨概要
- 巻号頁・発行日
- vol.31, pp.22, 2005
Clavubicyclone, a novel clavulone-related marine prostanoid, was isolated from Okinawan soft coral Clavularia viridis by our group. To determine the absolute stereochemistry of clavubicyclone, development of the total synthetic route was performed. The key step of our synthetic route was construction of bicyclo[3.2.1]octane skeleton by Cope rearrangement of the divinylcyclopropane derivative. The substrate of Cope rearrangement was prepared from cis-2-butene-1,4-diol as a starting material through carbon chain elongation reactions and the rhodium catalyzed intramolecular cyclopropanation reaction. The Cope rearrangement smoothly proceeded by heating the divinylcyclopropane derivative in diphenyl ether (180 °C) to give the desired bicyclo[3.2.1]octane derivative. We are examining to convert the rearrangement product to clavubicyclone.
1 0 0 0 クラブバイサイクロンの不斉合成研究
- 著者
- 渋谷 厚輝 武口 俊太 伊藤 久央 井口 和男
- 出版者
- 日本薬学会化学系薬学部会
- 雑誌
- 反応と合成の進歩シンポジウム 発表要旨概要
- 巻号頁・発行日
- vol.34, pp.144, 2008
Clavubicyclone was isolated from Okinawan soft coral, Clavularia viridis, by our group as a novel prostanoid-related compound. The absolute stereochemistry and biological activity of clavubicyclone have not yet been examined due to small quantities of isolated samples. We recently achieved the total synthesis of clavubicyclone as a racemic form through Cope rearrangement as a key step. However, there are several problems on our previous synthetic route; improvement of the yield of Cope rearrangement and shortening of the relatively longer sequence. To overcome these problems and to achieve an enantioselective synthesis, we examined further synthetic research. Cope rearrangement was proceeded smoothly by changing the stereochemistry of the substrate. We also achieved to obtain an intermediate as an optically active form by using enantioselective Mukaiyama aldol reaction. Introduction of side chains to an optically active bicyclo[3.2.1]octane skeleton is now underway.
1 0 0 0 タンパク質化学合成を指向したワンポット4成分連続縮合法の開発
- 著者
- 佐藤 浩平 津田 修吾 坂本 健 重永 章 大高 章
- 出版者
- 日本薬学会化学系薬学部会
- 雑誌
- 反応と合成の進歩シンポジウム 発表要旨概要
- 巻号頁・発行日
- vol.37, pp.180, 2011
Native chemical ligation (NCL), featuring the coupling of thioester peptides and N-terminal cysteinyl peptides, has shown great utility in chemical synthesis of a wide variety of proteins. Preparation of large proteins requires a sequential NCL using more than two peptide fragments. For this purpose, kinetically controlled NCL, developed by Kent and co-workers, has been preferentially used to yield much success in a sequential one-pot three-fragment coupling. In this study, we will report a more reliable alternate to the Kent's protocol with the use of an <I>N</I>-sulfanylethylanilide (SEAlide) peptide as a thioester equivalent. Furthermore, an unprecedented one-pot four-fragment coupling under kinetic conditions using a combination of our method and Kent's kinetic reaction will be also discussed.
1 0 0 0 リゼルグ酸および関連アルカロイドの不斉全合成
- 著者
- 岩田 顕 井貫 晋輔 大石 真也 藤井 信孝 大野 浩章
- 出版者
- 日本薬学会化学系薬学部会
- 雑誌
- 反応と合成の進歩シンポジウム 発表要旨概要
- 巻号頁・発行日
- vol.37, pp.164, 2011
The family of ergot alkaloids produced by the fungus <I>Claviceps purpurea</I> is one of the most intriguing classes of natural products because of their broad biological and pharmacological activities. Despite intensive synthetic investigations, most synthetic studies of the ergot alkaloids, particularly (+)-lysergic acid, (+)-lysergol and (+)-isolysergol, have relied on a stepwise linear approach for the construction of the C/D ring system. Recently, we developed a palladium-catalyzed domino cyclization of the racemic allenic amide to provide the tetracyclic core of ergot alkaloids. In this study, we constructed the chiral allenic amide via the two synthetic routes using aldehyde alkynylation/asymmetric hydrogenation or asymmetric epoxidation/regioselective reductive ring-opening reaction. Using the resulting chiral allenic amide , enantioselective total syntheses of (+)-lysergic acid, (+)-lysergol and (+)-isolysergol were accomplished.
1 0 0 0 ホウ素クラスターを骨格とする液晶性化合物の合成
- 著者
- 長峰 高志 太田 公規 遠藤 泰之 Januszko Adam Kaszynski Piotr
- 出版者
- 日本薬学会化学系薬学部会
- 雑誌
- 反応と合成の進歩シンポジウム 発表要旨概要
- 巻号頁・発行日
- vol.29, pp.58-59, 2003
典型的な液晶であるカラミティック液晶としての性質を示す分子の多くは、芳香環などの剛直な構造に、柔軟なアルキル鎖と分極性を与える極性官能基を組合わせた棒状の構造を有する。これらの構成部分の構造により、様々な性質を示すが、剛直な基本構造部分は安定性、色、誘電率、液晶相の温度範囲などの物性に大きな影響を与える。最近、芳香環に替えて2,2,2-bicyclooctane(BCO)を有する液晶性化合物が、研究されている。一方、<i>p</i>-カルボラン (1,12-dicarba-<i>closo</i>-dodecaborane) は二十面体構造の含ホウ素クラスター化合物であり、高い耐熱性と疎水性を有する。<i>p</i>-カルボランは、BCOと共通の球形の分子形状と直線的な置換基配向を有する上に、炭素上に容易に置換基を導入しうるというBCOにない合成上の利点をもつ。そこで、<i>p</i>-カルボランを基本骨格とする新規液晶分子の合成を目的として、図に例として示す化合物を含め10種の化合物を設計・合成して、その相転移を測定した。その結果、多くの化合物が明確にカラミティック液晶の一つであるネマティック液晶としての性質を示した。
- 著者
- 渡邉 一弘 成田 紘一 佐藤 静香 加藤 正
- 出版者
- 日本薬学会化学系薬学部会
- 雑誌
- 反応と合成の進歩シンポジウム 発表要旨概要
- 巻号頁・発行日
- vol.36, pp.139, 2010
In multistep syntheses of complex natural products, selection of the most suitable protecting group for each hydroxy function is very important and sometimes holds the key to success. We are interested in the chemoselective deprotection to expand synthetic applicability of phenyliodine(III) bis(trifluoroacetate) (PIFA). The hypervalent iodine reagent such as PIFA is one of the promising reagent for development of environmentally benign oxidations. We describe not only the deprotection of more readily removable 3,4-dimethoxybenxyl (<sup>3,4</sup>DMB) protecting groups, but also selectivity among the three benzyl-type protecting groups, <sup>3,4</sup>DMB, <I>p</I>-methoxybenzyl (PMB) and benzyl (Bn). When the tetra-protected compound (having Bn, PMB and <sup>3,4</sup>DMB groups) was treated with 2.0 equivalents of PIFA at room temperature, the <sup>3,4</sup>DMB group was removed to give mono-alcohol with more than 97% selectivity.
1 0 0 0 ナランタリドの全合成
- 著者
- 井上 宗宣 阿部 敏明 岩崎 克彦 加藤 正
- 出版者
- 日本薬学会化学系薬学部会
- 雑誌
- 反応と合成の進歩シンポジウム 発表要旨概要
- 巻号頁・発行日
- vol.29, pp.108-109, 2003
ナランタリド(<b>1</b>)は、2001年、メルク社のグループにより真菌(<i>Nalanthamala</i> sp. MF 5638)より単離、構造決定された電位依存性カリウムイオンチャンネルKv1.3阻害活性を示し、新しい作用機序を有する免疫抑制剤としての可能性が示唆されている天然有機化合物である。我々は、ナランタリド(<b>1</b>)の医薬的な価値に注目し、本化合物の効率的かつ柔軟性に富んだ合成法を開発することを主な目的として合成研究を開始した。今回、光学活性なナランタリドの全合成を初めて達成したのでその経緯につて報告する。 出発原料として光学活性なウィーランドミッシャーケトン類縁体(<b>2</b>)を用い、14段階を経てホモプレニル部を導入した化合物<b>3</b>を合成した。続いて、[<i>2, 3</i>]-Wittig転位(<b>3</b>→<b>4</b>)によりエキソオレフィン部の導入および5位の不斉中心を構築し、ピロン環(<b>6</b>)とのカップリング反応(<b>5</b>+<b>6</b>→<b>7</b>)を鍵段階として、光学活性なナランタリド(<b>1</b>)の合成に成功した(Scheme 1)。
1 0 0 0 OA アンセリジオーゲン-Anの合成研究
- 著者
- 高取 和彦 長澤 心 長岡 博人
- 出版者
- 日本薬学会化学系薬学部会
- 雑誌
- 反応と合成の進歩シンポジウム 発表要旨概要 第36回反応と合成の進歩シンポジウム
- 巻号頁・発行日
- pp.153, 2010 (Released:2010-11-03)
SmI2-induced cascade reaction involving reductive cyclization, Dieckmann condensation and lactonization has been developed in our laboratory, and applied to the total synthesis of (+-)-gibberellin A1. Herein, we report the further application of the reaction to the synthesis of antheridiogen-An, isolated from Anemia phyllitidis in 1971 by Nakanishi and coworkers, having unique tetracycic ring system with gamma-lactone. Our synthetic features for the challenging synthetic target were shown as follows. The CD ring was formed by SmI2-induced fragmentation reaction of the cyclopropane ring in the tricyclo[3.2.1.02,7]octane derivative, prepared by Michael-Michael-alkylation reaction. Formation of functionalized antheridane skeleton as a key step was achieved by application of the SmI2-induced reductive cyclization-Dieckmann condensation-lactonization of the keto diester as a intermediate.
1 0 0 0 OA 新規マイクロカプセル化オスミウム触媒を用いる不斉ジヒドロキシル化反応の開発
- 著者
- 石田 祐 秋山 良 小林 修
- 出版者
- 日本薬学会化学系薬学部会
- 雑誌
- 反応と合成の進歩シンポジウム 発表要旨概要 第29回反応と合成の進歩シンポジウム
- 巻号頁・発行日
- pp.44-45, 2003-09-24 (Released:2004-03-16)
四酸化オスミウム(OsO4)を用いるジヒドロキシル化反応は、オレフィンから1行程で連続する2つの不斉炭素を有するジオールを合成できることから、有機化学上最も重要な反応の一つである。当研究室では既にマイクロカプセル化法を用いることにより、ポリスチレンにOsO4を固定化し、触媒として回収・再使用可能であることを報告している。今回高分子担体の探索を行なった結果、poly(phenoxyethoxymethylstyrene-co-styrene)を担体として用いた新規マイクロカプセル化オスミウム触媒(PEM-MC OsO4)を開発し、二相系での不斉ジヒドロキシル化反応に適用可能であることを見出した。また興味深いことに、本触媒を疎水相とし、水のみを溶媒として用いる不斉ジヒドロキシル化反応が円滑に進行することを見出した。さらに筆者らは、新たに架橋型ポリスチレンを担体として用いマイクロカプセル化オスミウム触媒を合成し、この触媒が完全水中におけるオレフィンの不斉ジヒドロキシル化反応に対して高い触媒活性を示すことを見出した。架橋率の影響など詳細に関しても報告する。
1 0 0 0 OA ポリアミン部位を有するエンジインモデル化合物の合成とDNA切断活性
- 著者
- 重永 章 鈴木 一郎 根本 尚夫 渋谷 雅之
- 出版者
- 日本薬学会化学系薬学部会
- 雑誌
- 反応と合成の進歩シンポジウム 発表要旨概要 第29回反応と合成の進歩シンポジウム
- 巻号頁・発行日
- pp.178-179, 2003-09-24 (Released:2004-03-16)
抗腫瘍性抗生物質ネオカルチノスタチン(以下NCSと略記する)はMyers–Saito型の芳香環化反応によりビラジカルを生じ、このビラジカルがDNAを切断することにより、その生理活性が発現すると考えられている。ここで、活性種と考えられているデヒドロトルエンビラジカルは高いイオン性を有しており、水溶液中ではしばしばイオン的な反応を起こすために、DNA切断活性が低下するという問題点が指摘されている(図1)。我々のグループでは近年この問題点に取り組み、パイラジカル中心に電子吸引基を導入することによりイオン性を抑制した化合物が高いDNA切断活性を示すことを報告した(図2)。本講演では図3に示すようなDNA親和性部位としてポリアミン部位を導入したエンジインモデル化合物の合成、及びそのDNA切断活性について報告する。